Sebbene i nervi periferici siano in grado di rigenerarsi dopo un danno, il recupero è spesso incompleto negli anziani, nelle persone con patologie come il diabete o in seguito a traumi particolarmente gravi. Il sistema vascolare svolge un ruolo attivo nel sostegno alla riparazione nervosa, modellando il microambiente della guarigione e proteggendo il tessuto neurale attraverso la barriera emato-nervosa (BNB, dall'inglese blood-nerve barrier). Questa struttura neurovascolare specializzata è formata da vasi sanguigni che scorrono lungo le fibre assonali, all'interno dei nervi periferici, proteggendole da stress meccanici, sostanze tossiche e agenti nocivi. È ormai riconosciuto che l'alterazione della BNB è uno dei principali fattori alla base di dolore e neuropatia.
A differenza della più nota barriera ematoencefalica (BBB, blood-brain barrier), che protegge neuroni e cellule gliali nel cervello e nel midollo spinale, la BNB è storicamente poco studiata: i vasi sanguigni periferici sono pochi e difficilmente accessibili con le tecniche standard.

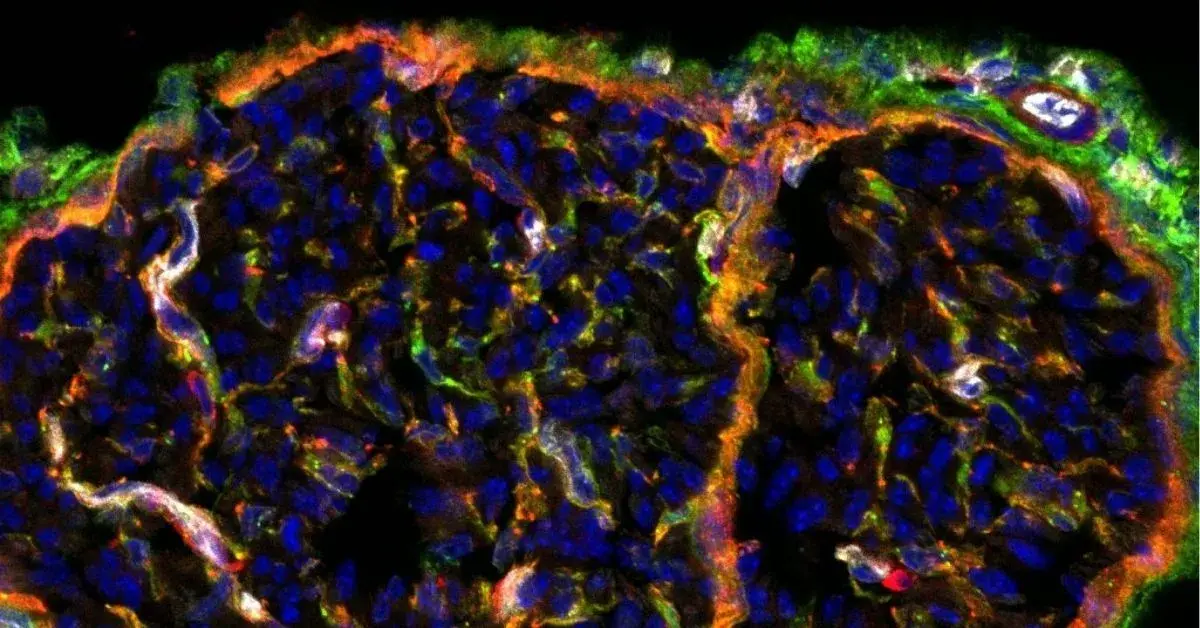
Sezione trasversale di nervo sciatico con i capillari che formano la BNB (in grigio) e le cellule dello stroma (ambiente circostante) evidenziate con i biomarcatori NG2 (in rosso) e PDGFRa (in verde). I nuclei sono in blu. Crediti: Dr. Dario Bonanomi
Che cos'è la barriera emato-nervosa e perché è importante
«Sappiamo poco sulla composizione cellulare e sulle proprietà molecolari della barriera emato-nervosa — spiega il dottor Dario Bonanomi, responsabile del Laboratorio di Neurobiologia Molecolare all'IRCCS Ospedale San Raffaele di Milano. Inoltre, non comprendiamo appieno la sua funzione nella rigenerazione nervosa dopo un danno, un processo che avviene tipicamente nel sistema nervoso periferico e non in quello centrale. Riteniamo che la BNB possa agire come un hub di segnalazione chimica e meccanica, centrale per la rigenerazione nervosa»
Bonanomi ha recentemente ricevuto un ERC Synergy Grant insieme ai gruppi di ricerca di Isabelle Brunet (Inserm, Francia), Tambet Teesalu (Università di Tartu, Estonia) ed Ellie Tzima (Università di Oxford, Regno Unito).
L'obiettivo del progetto è unire le forze per rispondere alle molte domande ancora aperte sulla BNB e studiarne il coinvolgimento nella rigenerazione del nervo periferico e nel dolore neuropatico indotto dai farmaci chemioterapici, un'esigenza clinica rimasta finora senza risposta.
Come la barriera emato-nervosa guida la rigenerazione del nervo periferico
Studi precedenti condotti dal dottor Bonanomi e dal suo gruppo hanno dimostrato che i vasi sanguigni nei nervi periferici sono indispensabili per il processo di rigenerazione. «Dopo un danno nervoso, i vasi formano impalcature polarizzate che guidano la ricrescita assonale. Se si distrugge la polarizzazione vascolare, la rigenerazione risulta compromessa» spiega Bonanomi.
«Quando i nervi periferici di un organismo adulto vengono danneggiati, i vasi attivano un programma di sviluppo necessario per la rigenerazione nervosa. In particolare, l'endotelio sovraregola il recettore Plexin-D1, che guida la migrazione assonale nel nervo in rigenerazione. Se si rimuove Plexin-D1 dai vasi del nervo danneggiato nell'adulto, la vascolarizzazione si disorganizza e non è più in grado di fornire i tracciati necessari per una rigenerazione nervosa guidata» aggiunge il ricercatore.
I vasi non sono però soltanto binari lungo cui migrano assoni e cellule di Schwann per attraversare il sito della lesione: sono anche hub di segnali molecolari che orchestrano la riparazione tissutale.
Il gruppo ha inoltre dimostrato che i vasi sanguigni che crescono nella ferita contribuiscono a modellare il tessuto circostante, istruendo cellule simil-fibroblastiche a formare "tunnel" protettivi attraverso cui si estendono gli assoni in rigenerazione.
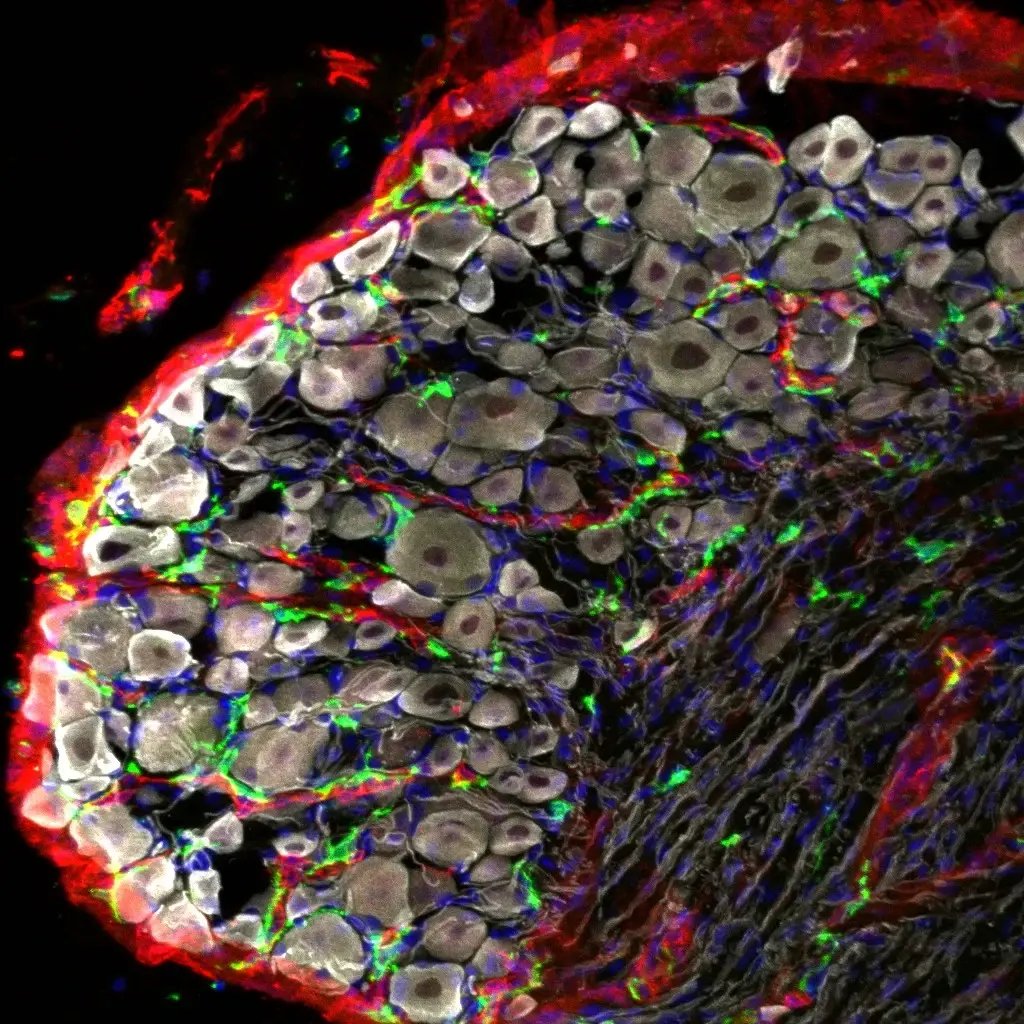
Ganglio sensoriale adulto che evidenzia i neuroni (in grigio), i vasi sanguigni (in rosso) e i macrofagi (in verde). I nuclei sono in blu. Crediti: Dr. Dario Bonanomi
MINerVA: quattro laboratori, un ERC Synergy Grant, tre domande aperte
Queste scoperte hanno confluito in uno sforzo collaborativo di ampia portata: il progetto MINerVA, sostenuto dall'ERC Synergy Grant. Il progetto mette insieme competenze complementari in segnalazione neurovascolare, peptidi homing in vivo e meccanotransduzione endoteliale, per rispondere a tre domande:
1. Come è organizzata la BNB?
2. Come risponde a un danno?
3. Come la disfunzione della BNB contribuisce alla malattia?
La trascrittomica single-cell e spaziale consente oggi ai ricercatori di studiare la composizione cellulare con una risoluzione molecolare senza precedenti. «Prevediamo di usare queste tecniche nel mio laboratorio per identificare le cellule che interagiscono con l'endotelio nella BNB» precisa Bonanomi.
Il gruppo punta, inoltre, a mappare il profilo molecolare dei vasi sanguigni periferici con i peptidi homing, una tecnologia sviluppata dal laboratorio del dottor Tambet Teesalu in Estonia.
«In questo contesto — spiega il dottor Bonanomi — i peptidi homing svolgeranno una doppia funzione: da un lato, come strumenti in grado di legarsi all'insieme dei recettori presenti sulla superficie dei vasi, contribuendo così a mapparne la diversità molecolare. Dall'altro, poiché questi peptidi sono progettati per attraversare la BNB, potranno anche essere usati come vettori per veicolare selettivamente farmaci attraverso la barriera emato-nervosa e raggiungere bersagli specifici nel nervo a fini terapeutici».
Forze meccaniche e barriera emato-nervosa: una nuova frontiera della ricerca
I nervi periferici percorrono la nostra pelle e i nostri muscoli e vengono quindi continuamente allungati e ruotati durante il movimento. Come preservano la propria integrità, e in particolare quella della BNB, sotto questo stress meccanico? E in che modo queste sollecitazioni influenzano la funzione e la rigenerazione del nervo periferico?
Con il contributo della dottoressa Ellie Tzima, esperta di meccanobiologia endoteliale, il gruppo MINerVA identificherà nuovi meccanocettori attivi nella barriera emato-nervosa, utilizzando una combinazione di saggi cellulari, approcci biochimici e nuovi modelli genetici murini che disaccoppiano le attività di segnalazione chimica e meccanica di questi recettori.
Capire come le cellule della BNB percepiscono e interpretano i segnali meccanici è il punto di convergenza tra ricerca di base e traslazionale.
Basandosi sui risultati del laboratorio di Isabelle Brunet, il gruppo esplorerà l'ipotesi che la neuropatia periferica da chemioterapia (CIPN), che colpisce circa il 90% dei pazienti trattati con farmaci a base di platino, possa derivare in parte da una vasocostrizione all'interno del nervo: uno stress meccanico che attiva in modo anomalo le fibre sensoriali e innesca il dolore.
«È qui che i peptidi homing potrebbero entrare in gioco come vettori: contiamo di sfruttare la loro capacità di attraversare la BNB per veicolare selettivamente farmaci che correggano la meccanosensibilità dell'endotelio nervoso e, potenzialmente, alleviare il dolore neuropatico» conclude il dottor Bonanomi.
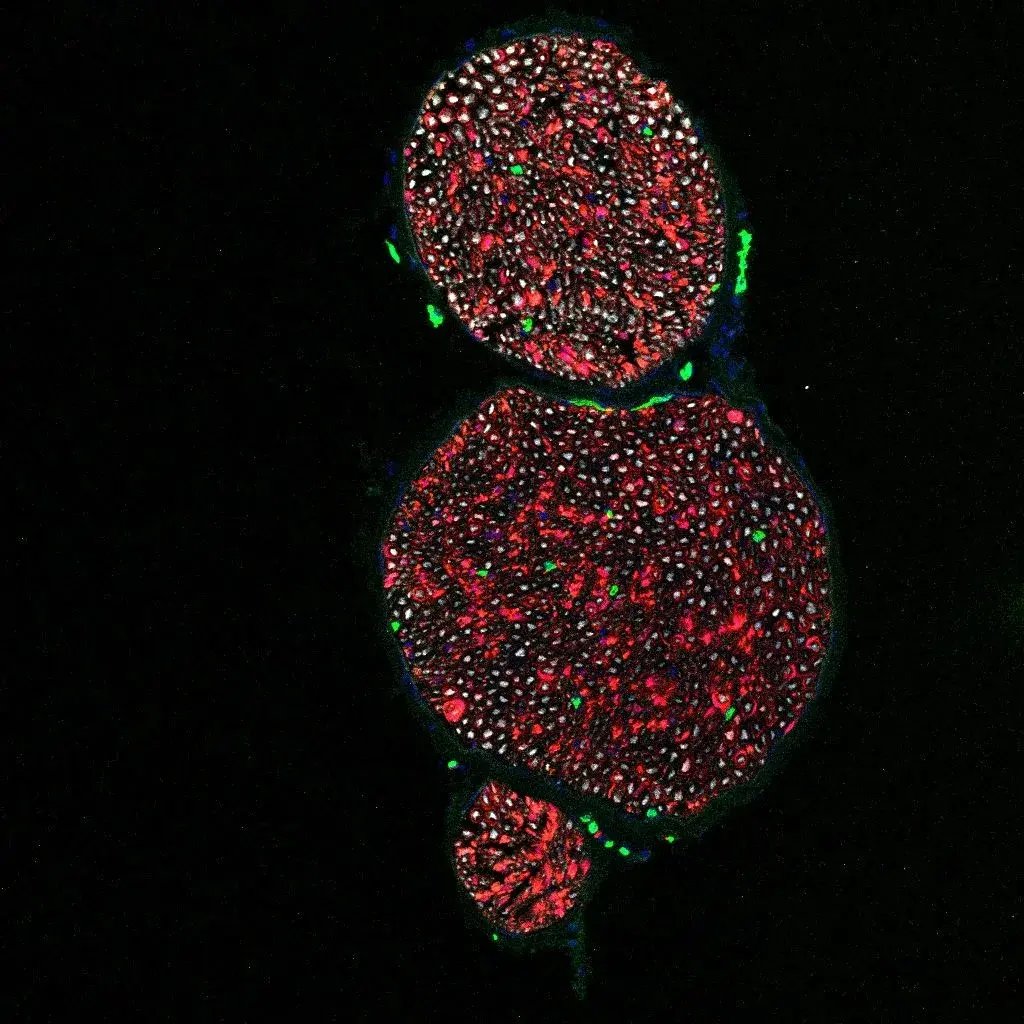
Sezione trasversale dei nervi periferici con i capillari (in verde) che formano la barriera emato-nervosa vicino agli assoni (in grigio) e le cellule di Schwann associate (in rosso). Crediti: Dr. Dario Bonanomi
Domande Frequenti sulla barriera emato-nervosa
Che cos'è la barriera emato-nervosa?
La barriera emato-nervosa è una struttura neurovascolare specializzata che si trova all'interno dei nervi periferici. È formata da vasi sanguigni che scorrono lungo le fibre assonali, creando una barriera selettiva che protegge il tessuto nervoso da stress meccanici, sostanze tossiche e agenti nocivi in circolo nel sangue. La sua funzione è in parte analoga a quella della barriera ematoencefalica nel sistema nervoso centrale, ma opera in un contesto anatomico molto diverso.
Perché la barriera emato-nervosa è stata così difficile da studiare?
A differenza del cervello, dove i vasi sanguigni sono numerosi e relativamente accessibili, i nervi periferici contengono pochi vasi, difficili da isolare e analizzare con le tecniche di laboratorio standard. Questo ha limitato fino ad oggi la capacità dei ricercatori di caratterizzare la composizione cellulare e le proprietà molecolari della BNB, lasciando senza risposta domande fondamentali sul suo ruolo nella riparazione nervosa e nella malattia.
Cosa accade alla barriera emato-nervosa dopo un danno nervoso?
Dopo una lesione del nervo periferico, i vasi sanguigni all'interno del nervo attivano un programma di sviluppo che sostiene la rigenerazione. Formano impalcature polarizzate che guidano la ricrescita assonale e rilasciano segnali molecolari che istruiscono le cellule circostanti a costruire tunnel protettivi attraverso cui si estendono gli assoni in rigenerazione. Quando questa risposta vascolare viene alterata, la rigenerazione nervosa risulta compromessa.